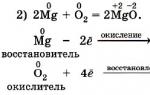Окислительно-восстановительные реакции. По изменению степени окисления все химические реакции можно разделить на два типа
По признаку изменения степеней окисления атомов, входящих в состав реагирующих веществ, химические реакции подразделяются на два типа.
1) Реакции, протекающие без изменения степеней окисления атомов.
Например:
2+4-2 t +2 -2 +4 -2
CaCO 3 = CaO + CO 2
В этой реакции степень окисления каждого из атомов осталась без изменения.
2) Реакции, протекающие с изменением степеней окисления атомов.
Например:
0 +2 -1 0 +2 -1
Zn + CuCl 2 = Cu + ZnCl 2
В этой реакции степени окисления атомов цинка и меди изменились.
Окислительно-восстановительные реакции – наиболее распространенные химические реакции.
На практике окислительно-восстановительная реакция – это присоединение или отдача электронов. Одни атомы (ионы, молекулы) отдают другим или принимают от них электроны.
Окисление.
Процесс отдачи электронов атомом, ионом или молекулой называется окислением .
При отдаче электронов степень окисления атома повышается.
Вещество, чьи атомы, ионы или молекулы отдают электроны, называется восстановителем .
В нашем примере атомы в степени окисления 0 перешли в атомы со степенью окисления +2. То есть произошел процесс окисления. При этом атом цинка, отдавший два электрона, является восстановителем (он повысил степень окисления с 0 до +2).
Процесс окисления записывают электронным уравнением, в котором указывают изменение степени окисления атомов и число электронов, отданных восстановителем.
Например:
0 +2 0
Zn – 2e – = Zn (окисление, Zn – восстановитель).
Восстановление.
Процесс присоединения электронов называют восстановлением .
При присоединении электронов степень окисления атома понижается.
Вещество, чьи атомы, ионы или молекулы присоединяют электроны, называют окислителем .
В нашем примере переход атомов меди со степенью окисления +2 в атомы со степенью окисления 0 является процессом восстановления. При этом атом меди со степенью окисления +2, принимая два электрона, понижает степень окисления от +2 до 0 и является окислителем.
Процесс окисления тоже записывают электронным уравнением:
2 0 0
Cu + 2e – = Cu (восстановление, Cu – окислитель).
Процесс восстановления и процесс окисления нераздельны и протекают одновременно.
0 +2 0 +2
Zn + CuCl 2 = Cu + ZnCl 2
восстановитель окислитель
окисляется восстанавливается
Окислительно-восстановительные реакции (ОВР) – реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ, в результате переноса электронов от одного атома к другому.
Степень окисления – формальный заряд атома в молекуле,вычисленный исходя из предположения, что молекула состоит только от ионов.
Наиболее электроотрицательные элементы в соединении имеют отрицательные степени окисления, а атомы элементов с меньшей электроотрицательностью − положительные.
Степень окисления − формальное понятие; в ряде случаев степень окисления не совпадает с валентностью.
Например: N 2 H 4 (гидразин)
степень окисления азота – -2; валентность азота – 3.
Расчет степени окисления
Для вычисления степени окисления элемента следует учитывать следующие положения:
1. Степени окисления атомов в простых веществах равны нулю (Na 0 ; H 2 0).
2. Алгебраическая сумма степеней окисления всех атомов, входящих в состав молекулы, всегда равна нулю, а в сложном ионе эта сумма равна заряду иона.
3. Постоянную степень окисления имеют атомы: щелочных металлов (+1), щелочноземельных металлов (+2), водорода (+1) (кроме гидридов NaH, CaH 2 и др., где степень окисления водорода -1), кислорода (-2) (кроме F 2 -1 O +2 и пероксидов, содержащих группу –O–O–, в которой степень окисления кислорода -1).
4. Для элементов положительная степень окисления не может превышать величину, равную номеру группы периодической системы.
V 2 +5 O 5 -2 ; Na 2 +1 B 4 +3 O 7 -2 ; K +1 Cl +7 O 4 -2 ; N -3 H 3 +1 ; K 2 +1 H +1 P +5 O 4 -2 ; Na 2 +1 Cr 2 +6 O 7 -2
Реакции с изменением, и без изменения степени окисления
Существует два типа химических реакций:
A Реакции, в которых не изменяется степень окисления элементов:
Реакции присоединения: SO 2 + Na 2 O Na 2 SO 3
Реакции разложения: Cu(OH) 2 CuO + H 2 O
Реакции обмена: AgNO 3 + KCl AgCl +KNO 3
NaOH + HNO 3 NaNO 3 + H 2 O
B Реакции, в которых происходит изменение степеней окисления атомов элементов, входящих в состав реагирующих соединений:
2Mg 0 + O 2 0 2Mg +2 O -2
2KCl +5 O 3 -2 – t 2KCl -1 + 3O 2 0
2KI -1 + Cl 2 0 2KCl -1 + I 2 0
Mn +4 O 2 + 4HCl -1 Mn +2 Cl 2 + Cl 2 0 + 2H 2 O
Такие реакции называются окислительно-восстановительными.
Окисление, восстановление
В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим. Процесс отдачи электронов - окисление . При окислении степень окисления повышается:
H 2 0 − 2ē 2H +
S -2 − 2ē S 0
Al 0 − 3ē Al +3
Fe +2 − ē Fe +3
2Br - − 2ē Br 2 0
Процесс присоединения электронов -− восстановление . При восстановлении степень окисления понижается.
Mn +4 + 2ē Mn +2
Сr +6 +3ē Cr +3
Cl 2 0 +2ē 2Cl -
O 2 0 + 4ē 2O -2
Атомы или ионы, которые в данной реакции присоединяют электроны, являются окислителями, а которые отдают электроны - восстановителями.
Окислительно-восстановительные свойства вещества и степени окисления входящих в него атомов
Соединения, содержащие атомы элементов с максимальной степенью окисления, могут быть только окислителями за счет этих атомов, т.к. они уже отдали все свои валентные электроны и способны только принимать электроны. Максимальная степень окисления атома элемента равна номеру группы в периодической таблице, к которой относится данный элемент. Соединения, содержащие атомы элементов с минимальной степенью окисления могут служить только восстановителями, поскольку они способны лишь отдавать электроны, потому, что внешний энергетический уровень у таких атомов завершен восемью электронами. Минимальная степень окисления атомов металлов равна 0, для неметаллов - (n–8) (где n- номер группы в периодической системе). Соединения, содержащие атомы элементов с промежуточной степенью окисления, могут быть и окислителями и восстановителями, в зависимости от партнера, с которым взаимодействуют и от условий реакции.
Задание №1
Установите соответствие между уравнением реакции и свойством элемента азота, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 4221
Пояснение:
А) NH 4 HCO 3 – соль, в состав которой входит катион аммония NH 4 + . В катионе аммония азот всегда имеет степень окисления, равную -3. В результате реакции он превращается в аммиак NH 3 . Водород практически всегда (кроме его соединений с металлами) имеет степень окисления, равную +1. Поэтому, чтобы молекула аммиака была электронейтральной, азот должен иметь степень окисления, равную -3. Таким образом, изменения степени окисления азота не происходит, т.е. он не проявляет окислительно-восстановительных свойств.
Б) Как уже было показано выше, азот в аммиаке NH 3 имеет степень окисления -3. В результате реакции с CuO аммиак превращается в простое вещество N 2 . В любом простом веществе степень окисления элемента, которым оно образовано, равна нулю. Таким образом, атом азота теряет свой отрицательный заряд, а поскольку за отрицательный заряд отвечают электроны, это означает их потерю атомом азота в результате реакции. Элемент, который в результате реакции теряет часть своих электронов, называется восстановителем.
В) В результате реакции NH 3 со степенью окисления азота, равной -3, превращается в оксид азота NO. Кислород практически всегда имеет степень окисления, равную -2. Поэтому для того, чтобы молекула оксида азота была электронейтральной, атом азота должен иметь степень окисления +2. Это означает, что атом азота в результате реакции изменил свою степень окисления с -3 до +2. Это говорит о потере атомом азота 5 электронов. То есть азот, как и случает Б, является восстановителем.
Г) N 2 – простое вещество. Во всех простых веществах элемент, который их образует, имеет степень окисления, равную 0. В результате реакции азот превращается в нитрид лития Li3N. Единственная степень окисления щелочного металла, кроме нуля (степень окисления 0 бывает у любого элемента), равна +1. Таким образом, чтобы структурная единица Li3N была электронейтральной, азот должен иметь степень окисления, равную -3. Получается, что в результате реакции азот приобрел отрицательный заряд, что означает присоединение электронов. Азот в данной реакции окислитель.
Задание №2
Установите соответствие между схемой реакции и свойством элемента фосфора, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 1224
Задание №3
| УРАВНЕНИЕ РЕАКЦИИ | |
| А) 4NH 3 + 5O 2 → 4NO + 6H 2 O Б) 2Cu(NO 3) 2 → 2CuO + 4NO 2 + O 2 В) 4Zn + 10HNO 3 → NH 4 NO 3 + 4Zn(NO 3) 2 + 3H 2 O Г) 3NO 2 + H 2 O → 2HNO 3 + NO |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 1463
Задание №4
Установите соответствие между уравнением реакции и изменением степени окисления окислителя в ней: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ |
| А) SO 2 + NO 2 → SO 3 + NO Б) 2NH 3 + 2Na → 2NaNH 2 + H 2 В) 4NO 2 + O 2 + 2H 2 O → 4HNO 3 Г) 4NH 3 + 6NO → 5N 2 + 6H 2 O |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 3425
Задание №5
Установите соответствие между схемой реакции и коэффициентом перед окислителем в ней: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | КОЭФФИЦИЕНТ ПЕРЕД ОКИСЛИТЕЛЕМ |
| А) NH 3 + O 2 → N 2 + H 2 O Б) Cu + HNO 3 (конц.) → Cu(NO 3) 2 + NO 2 + H 2 O В) C + HNO 3 → NO 2 + CO 2 + H 2 O Г) S + HNO 3 →H 2 SO 4 + NO |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 3442
Задание №6
Установите соответствие между уравнением реакции и изменением степени окисления окислителя в ней: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ |
| А) 2NH 3 + K → 2KNH 2 + H 2 Б) H 2 S + K → K 2 S + H 2 В) 4NH 3 + 6NO → 5N 2 + 6H 2 O Г) 2H 2 S + 3O 2 → 2SO 2 + 2H 2 O |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 4436
Задание №7
Установите соответствие между исходными веществами и свойством меди, которое этот элемент проявляет в данной реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 2124
Задание №8
Установите соответствие между схемой реакции и свойством серы, которое она проявляет в данной реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 3224
Задание №9
Установите соответствие между схемой реакции и свойством фосфора, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 3242
Задание №10
Установите соответствие между схемой реакции и свойством азота, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 2141
Задание №11
Установите соответствие между схемой реакции и свойством фтора, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 1444
Задание №12
Установите соответствие между схемой реакции и изменением степени окисления восстановителя: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | |
| А) NaIO → NaI + NaIO 3 Б) HI + H 2 O 2 → I 2 + H 2 O В) NaIO 3 → NaI + O 2 Г) NaIO 4 → NaI + O 2 | 1) I +5 → I −1 2) O −2 → O 0 3) I +7 →I −1 4) I +1 → I −1 5) I +1 → I +5 6) I −1 → I 0 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 5622
Задание №13
Установите соответствие между уравнением реакции и изменением степени окисления восстановителя в данной реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ВОССТАНОВИТЕЛЯ |
| А) H 2 S + I 2 → S + 2HI Б) Cl 2 + 2HI → I 2 + 2HCl В) 2SO 3 + 2KI → I 2 + SO 2 + K 2 SO 4 Г) S + 3NO 2 → SO 3 + 3NO |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 5331
Задание №14
Установите соответствие между уравнением окислительно-восстановительной реакции и изменением степени окисления серы в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ СЕРЫ |
| А) S + O 2 → SO 2 Б) SO 2 + Br 2 + 2H 2 O → H 2 SO 4 + 2HBr В) C + H 2 SO 4 (конц.) → CO 2 + 2SO 2 + 2H 2 O Г) 2H 2 S + O 2 → 2H 2 O + 2S |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 4123
Задание №15
| ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ | ФОРМУЛЫ ВЕЩЕСТВ |
| А) S −2 → S +4 Б) S −2 → S +6 В) S +6 → S −2 Г) S −2 → S 0 | 1) Cu 2 S и O 2 2) H 2 S и Br 2 (р-р) 3) Mg и H 2 SO 4 (конц.) 4) H 2 SO 3 и O 2 5) PbS и HNO 3 (конц.) 6) C и H 2 SO 4 (конц.) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 1532
Задание №16
Установите соответствие между изменением степени окисления серы в реакции и формулами исходных веществ, которую в нее вступают: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ | ФОРМУЛЫ ВЕЩЕСТВ |
| А) S 0 → S +4 Б) S +4 → S +6 В) S −2 → S 0 Г) S +6 → S +4 | 1) Cu и H 2 SO 4 (разб.) 2) H 2 S и O 2 (недост.) 3) S и H 2 SO 4 (конц.) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 3523
Задание №17
Установите соответствие между свойствами азота и уравнением окислительно-восстановительной реакции, в которой он проявляет эти свойства: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 2143
Задание №18
Установите соответствие между изменением степени окисления хлора в реакции и формулами исходных веществ, которую в нее вступают: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ | ФОРМУЛЫ ИСХОДНЫХ ВЕЩЕСТВ |
| А) Cl 0 → Cl −1 Б) Cl −1 → Cl 0 В) Cl +5 → Cl −1 Г) Cl 0 → Cl +5 | 1) KClO 3 (нагревание) 2) Cl 2 и NaOH(горяч. р-р) 3) KCl и H 2 SO 4 (конц.) 6) KClO 4 и H 2 SO 4 (конц.) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 2412
Задание №19
Установите соответствие между формулой иона и его способностью проявлять окислительно-восстановительные свойства: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 2332
Задание №20
Установите соответствие между схемой химической реакции и изменением степени окисления окислителя: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ОКИСЛИТЕЛЯ |
| А) MnCO 3 + KClO 3 → MnO 2 + KCl + CO 2 Б) Cl 2 + I 2 + H 2 O → HCl + HIO 3 В) H 2 MnO 4 → HMnO 4 + MnO 2 + H 2 O Г) Na 2 SO 3 + KMnO 4 + KOH → Na 2 SO 4 + K 2 MnO 4 + H 2 O | 1) Cl 0 → Cl − 2) Mn +6 → Mn +4 3) Cl +5 → Cl − 4) Mn +7 → Mn +6 5) Mn +2 → Mn +4 6) S +4 → S +6 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ: 3124
Задание №21
Установите соответствие между схемой реакции и изменением степени окисления восстановителя в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
По этому признаку различают окислительно-восстановительные реакции и реакции, протекающие без изменения степеней окисления химических элементов.
К ним относится множество реакций, в том числе все реакции замещения, а также те реакции соединения и разложения, в которых участвует хотя бы одно простое вещество, например:

Как вы помните, коэффициенты в сложных окислительно-восстановительных реакциях расставляют, используя метод электронного баланса:

В органической химии ярким примером окислительно-восстановительных реакций могут служить свойства альдегидов.
1. Они восстанавливаются в соответствующие спирты:

2. Альдегиды окисляются в соответствующие кислоты:


Сущность всех приведенных выше примеров окислительно-восстановительных реакций была представлена с помощью хорошо известного вам метода электронного баланса. Он основан на сравнении степеней окисления атомов в реагентах и продуктах реакции и на балансировании числа электронов в процессах окисления и восстановления. Этот метод применяют для составления уравнений реакций, протекающих в любых фазах. Этим он универсален и удобен. Но в то же время он имеет серьезный недостаток - при выражении сущности окислительно-восстановительных реакций, протекающих в растворах, указываются частицы, которые реально не существуют.
В этом случае удобнее использовать другой метод - метод полуреакций. Он основан на составлении ионноэлектронных уравнений для процессов окисления и восстановления с учетом реально существующих частиц и последующем суммировании их в общее уравнение. В этом методе не используют понятие «степень окисления», а продукты определяются при выводе уравнения реакции.
Продемонстрируем этот метод на примере: составим уравнение окислительно-восстановительной реакции цинка с концентрированной азотной кислотой.
1. Записываем ионную схему процесса, которая включает только восстановитель и продукт его окисления, окислитель и продукт его восстановления:
2. Составляем ионно-электронное уравнение процесса окисления (это 1-я полуреакция):
3. Составляем ионно-электронное уравнение процесса восстановления (это 2-я полуреакция):
Обратите внимание: электронно-ионные уравнения составляются в соответствии с законом сохранения массы и заряда.
4. Записываем уравнения полуреакций так, чтобы число электронов между восстановителем и окислителем было сбалансированно:
5. Суммируем почленно уравнения полуреакций. Составляем общее ионное уравнение реакции:
Проверяем правильность составления уравнения реакции в ионном виде:
- Соблюдение равенства по числу атомов элементов и по числу зарядов
- Число атомов элементов должно быть равно в левой и правой частях ионного уравнения реакции.
- Общий заряд частиц в левой и правой частях ионного уравнения должен быть одинаков.
6. Записываем уравнение в молекулярной форме. Для этого добавляем к ионам, входящим в ионное уравнение, необходимое число ионов противоположного заряда.
ОПРЕДЕЛЕНИЕ
Степень окисления - это количественная оценка состояния атома химического элемента в соединении, основанная на его электроотрицательности.
Она принимает как положительные, так и отрицательные значения. Чтобы указать степень окисления элемента в соединении нужно поставить сверху над его символом арабскую цифру с соответствующим знаком («+» или «-»).
Следует помнить, что степень окисления — величина, не имеющая физического смысла, так как не отражает реальный заряд атома. Однако это понятие весьма широко используется в химии.
Таблица степени окисления химических элементов
Максимальную положительную и минимальную отрицательную степень окисления можно определить с помощью Периодической таблицы Д.И. Менделеева. Они равны номеру группы, в которой расположен элемент, и разнице между значением «высшей» степени окисления и числом 8, соответственно.
Если рассматривать химические соединения более конкретно, то в веществах с неполярными связями степень окисления элементов равна нулю (N 2 , H 2 , Cl 2).
Степень окисления металлов в элементарном состоянии равна нулю, так как распределение электронной плотности в них равномерно.
В простых ионных соединениях степень окисления входящих в них элементов равна электрическому заряду, поскольку при образовании этих соединений происходит практически полный переход электронов от одного атома к другому: Na +1 I -1 , Mg +2 Cl -1 2 , Al +3 F -1 3 , Zr +4 Br -1 4 .
При определении степени окисления элементов в соединениях с полярными ковалентными связями сравнивают значениях их электроотрицательностей. Поскольку при образовании химической связи электроны смещаются к атомам более электроотрицательных элементов, то последние имеют в соединениях отрицательную степень окисления.
Существуют элементы, для которых характерно только одно значение степени окисления (фтор, металлы IA и IIA групп и т.д.). Фтор, характеризующийся наибольшим значением электроотрицательности, в соединениях всегда имеет постоянную отрицательную степень окисления (-1).
Щелочные и щелочноземельные элементы, для которых свойственно относительно невысокое значение электроотрицательности, всегда имеют положительную степень окисления, равную соответственно (+1) и (+2).
Однако, имеются и такие химические элементы, для которых характерны несколько значений степени окисления (сера - (-2), 0, (+2), (+4), (+6) и др.).
Для того, чтобы легче было запомнить сколько и какие степени окисления характерны для конкретного химического элемента используют таблицы степеней окисления химических элементов, которые выглядят следующим образом:
|
Порядковый номер |
Русское / англ. название |
Химический символ |
Степень окисления |
|
Водород / Hydrogen |
|||
|
Гелий / Helium |
|||
|
Литий / Lithium |
|||
|
Бериллий / Beryllium |
|||
|
(-1), 0, (+1), (+2), (+3) |
|||
|
Углерод / Carbon |
(-4), (-3), (-2), (-1), 0, (+2), (+4) |
||
|
Азот / Nitrogen |
(-3), (-2), (-1), 0, (+1), (+2), (+3), (+4), (+5) |
||
|
Кислород / Oxygen |
(-2), (-1), 0, (+1), (+2) |
||
|
Фтор / Fluorine |
|||
|
Натрий / Sodium |
|||
|
Магний / Magnesium |
|||
|
Алюминий / Aluminum |
|||
|
Кремний / Silicon |
(-4), 0, (+2), (+4) |
||
|
Фосфор / Phosphorus |
(-3), 0, (+3), (+5) |
||
|
Сера / Sulfur |
(-2), 0, (+4), (+6) |
||
|
Хлор / Chlorine |
(-1), 0, (+1), (+3), (+5), (+7), редко (+2) и (+4) |
||
|
Аргон / Argon |
|||
|
Калий / Potassium |
|||
|
Кальций / Calcium |
|||
|
Скандий / Scandium |
|||
|
Титан / Titanium |
(+2), (+3), (+4) |
||
|
Ванадий / Vanadium |
(+2), (+3), (+4), (+5) |
||
|
Хром / Chromium |
(+2), (+3), (+6) |
||
|
Марганец / Manganese |
(+2), (+3), (+4), (+6), (+7) |
||
|
Железо / Iron |
(+2), (+3), редко (+4) и (+6) |
||
|
Кобальт / Cobalt |
(+2), (+3), редко (+4) |
||
|
Никель / Nickel |
(+2), редко (+1), (+3) и (+4) |
||
|
Медь / Copper |
+1, +2, редко (+3) |
||
|
Галлий / Gallium |
(+3), редко (+2) |
||
|
Германий / Germanium |
(-4), (+2), (+4) |
||
|
Мышьяк / Arsenic |
(-3), (+3), (+5), редко (+2) |
||
|
Селен / Selenium |
(-2), (+4), (+6), редко (+2) |
||
|
Бром / Bromine |
(-1), (+1), (+5), редко (+3), (+4) |
||
|
Криптон / Krypton |
|||
|
Рубидий / Rubidium |
|||
|
Стронций / Strontium |
|||
|
Иттрий / Yttrium |
|||
|
Цирконий / Zirconium |
(+4), редко (+2) и (+3) |
||
|
Ниобий / Niobium |
(+3), (+5), редко (+2) и (+4) |
||
|
Молибден / Molybdenum |
(+3), (+6), редко (+2), (+3) и (+5) |
||
|
Технеций / Technetium |
|||
|
Рутений / Ruthenium |
(+3), (+4), (+8), редко (+2), (+6) и (+7) |
||
|
Родий / Rhodium |
(+4), редко (+2), (+3) и (+6) |
||
|
Палладий / Palladium |
(+2), (+4), редко (+6) |
||
|
Серебро / Silver |
(+1), редко (+2) и (+3) |
||
|
Кадмий / Cadmium |
(+2), редко (+1) |
||
|
Индий / Indium |
(+3), редко (+1) и (+2) |
||
|
Олово / Tin |
(+2), (+4) |
||
|
Сурьма / Antimony |
(-3), (+3), (+5), редко (+4) |
||
|
Теллур / Tellurium |
(-2), (+4), (+6), редко (+2) |
||
|
(-1), (+1), (+5), (+7), редко (+3), (+4) |
|||
|
Ксенон / Xenon |
|||
|
Цезий / Cesium |
|||
|
Барий / Barium |
|||
|
Лантан / Lanthanum |
|||
|
Церий / Cerium |
(+3), (+4) |
||
|
Празеодим / Praseodymium |
|||
|
Неодим / Neodymium |
(+3), (+4) |
||
|
Прометий / Promethium |
|||
|
Самарий / Samarium |
(+3), редко (+2) |
||
|
Европий / Europium |
(+3), редко (+2) |
||
|
Гадолиний / Gadolinium |
|||
|
Тербий / Terbium |
(+3), (+4) |
||
|
Диспрозий / Dysprosium |
|||
|
Гольмий / Holmium |
|||
|
Эрбий / Erbium |
|||
|
Тулий / Thulium |
(+3), редко (+2) |
||
|
Иттербий / Ytterbium |
(+3), редко (+2) |
||
|
Лютеций / Lutetium |
|||
|
Гафний / Hafnium |
|||
|
Тантал / Tantalum |
(+5), редко (+3), (+4) |
||
|
Вольфрам / Tungsten |
(+6), редко (+2), (+3), (+4) и (+5) |
||
|
Рений / Rhenium |
(+2), (+4), (+6), (+7), редко (-1), (+1), (+3), (+5) |
||
|
Осмий / Osmium |
(+3), (+4), (+6), (+8), редко (+2) |
||
|
Иридий / Iridium |
(+3), (+4), (+6), редко (+1) и (+2) |
||
|
Платина / Platinum |
(+2), (+4), (+6), редко (+1) и (+3) |
||
|
Золото / Gold |
(+1), (+3), редко (+2) |
||
|
Ртуть / Mercury |
(+1), (+2) |
||
|
Талий / Thallium |
(+1), (+3), редко (+2) |
||
|
Свинец / Lead |
(+2), (+4) |
||
|
Висмут / Bismuth |
(+3), редко (+3), (+2), (+4) и (+5) |
||
|
Полоний / Polonium |
(+2), (+4), редко (-2) и (+6) |
||
|
Астат / Astatine |
|||
|
Радон / Radon |
|||
|
Франций / Francium |
|||
|
Радий / Radium |
|||
|
Актиний / Actinium |
|||
|
Торий / Thorium |
|||
|
Проактиний / Protactinium |
|||
|
Уран / Uranium |
(+3), (+4), (+6), редко (+2) и (+5) |
Примеры решения задач
ПРИМЕР 1
- Степень окисления фосфора в фосфине равна (-3), а в ортофосфорной кислоте - (+5). Изменение степени окисления фосфора: +3 → +5, т.е. первый вариант ответа.
- Степень окисления химического элемента в простом веществе равна нулю. Степень окисления фосфора в оксиде состава P 2 O 5 равна (+5). Изменение степени окисления фосфора: 0 → +5, т.е. третий вариант ответа.
- Степень окисления фосфора в кислоте состава HPO 3 равна (+5), а H 3 PO 2 — (+1). Изменение степени окисления фосфора: +5 → +1, т.е. пятый вариант ответа.
ПРИМЕР 2
| Задание | Степень окисления (-3) углерод имеет в соединении: а) CH 3 Cl; б) C 2 H 2 ; в) HCOH; г) C 2 H 6 . |
| Решение | Для того, чтобы дать верный ответ на поставленный вопрос будем поочередно определять степень окисления углерода в каждом из предложенных соединений.
а) степень окисления водорода равна (+1), а хлора - (-1). Примем за «х» степень окисления углерода: x + 3×1 + (-1) =0; Ответ неверный. б) степень окисления водорода равна (+1). Примем за «у» степень окисления углерода: 2×у + 2×1 = 0; Ответ неверный. в) степень окисления водорода равна (+1), а кислорода - (-2). Примем за «z» степень окисления углерода: 1 + z + (-2) +1 = 0: Ответ неверный. г) степень окисления водорода равна (+1). Примем за «a» степень окисления углерода: 2×а + 6×1 = 0; Верный ответ. |
| Ответ | Вариант (г) |